

Ученые выяснили, что триметиламиноксид (ТМАО), который образуется в печени из продуктов жизнедеятельности кишечного микробиома, провоцирует окислительный стресс, который приводит к эндотелиальной дисфункции сосудов. Как отмечается в статье, опубликованной в журнале Hypertension, с возрастом концентрация ТМАО в плазме повышается, что и ведет к инактивации эндотелиальной синтазы оксида азота и активации окислительного стресса. Оба этих процесса напрямую способствуют эндотелиальной дисфункции, которая запускает процессы атеросклероза.
Эндотелиальная дисфункция — важный предвестник и ранний маркер атеросклероза, который участвует в патогенезе большинства сердечно-сосудистых заболеваний. При таком состоянии клетки эндотелия (вид эпителия, покрывающий сосуды изнутри) хуже синтезируют важные гуморальные вещества, контролирующие состояние крови и самих сосудов: факторы свертываемости и регуляторы тонуса сосудов, важнейшим из которых является эндотелиальная синтаза оксида азота (eNOS). Оксид азота расслабляет гладкие мышцы сосудов, из-за чего они расширяются и артериальное давление падает. Если его синтез нарушен, сосуды не способны расслабляться и кровяное давление остается повышенным, что увеличивает риск развития сердечно-сосудистых заболеваний.
Группа ученых под руководством Дугласа Силса (Douglas R. Seals) из Университета Колорадо в Боулдере исследовала, как концентрация триметиламиноксида в плазме крови меняется с возрастом, и какое действие он оказывает на сосуды. ТМАО образуется в печени из предшественника — триметиламина (ТМА). Его, в свою очередь, синтезирует кишечная микрофлора — из холина, L-карнитина (витаминоподобные вещества B4) и бетаина, поступающих из пищи.
Предыдущие исследования показали, что концентрация ТМАО в плазме крови выше у старых самцов мышей (26-28 месяцев) по сравнению с молодыми (6-8 месяцев). Для контроля настоящего исследования одну группу молодых самцов мышей кормили холиновой диетой, другую — с содержанием 0,12 процента TMAO в течение 6 месяцев. Контрольную группу кормили обычным кормом. Концентрация ТМАО в плазме крови была достоверно повышена у мышей, получавших ТМАО (31,5 ± 9,5 микромоля на литр) по сравнению с контролем (2,9 ± 0,4 микромоля на литр, р < 0,05), но ТМАО не влиял на концентрацию предшественников ТМАО в плазме крови (р > 0,45). Добавление ТМАО также не влияло на массу тела, аппетит и массу ключевых органов (р > 0,27).
Эндотелий-зависимое расширение сосуда происходит под действием вырабатываемого эндотелием оксида азота. Такое расширение сонной артерии при возрастающих дозах ацетилхолина (нейромедиатор, запускающий синтез оксида азота в эндотелии) было достоверно ниже в группе с добавкой ТМАО (р < 0,01). Ученые выяснили, что такое расширение сосудов напрямую связана со сниженной биодоступностью оксида азота.
Ученые предположили, что снижение биодоступности оксида азота может быть связано либо со снижением его производства эндотелиальной синтазой оксида азота, либо с его повышенным разрушением в реакциях оксидативного стресса. Они обнаружили, что содержание фосфорилированного eNOS, хорошо зарекомендовавшего себя маркера активной формы фермента, было ниже в аортах мышей с добавлением TMAO по сравнению с контролем (р < 0,05). Содержание нитротирозина — индикатора окислительной модификации остатков тирозина в белках и маркера окислительного стресса — также было разным в двух группах мышей. В аортах мышей, которых кормили пищей с добавками ТМАО, нитротирозина было в 2 раза больше, чем у мышей из контрольной группы (р < 0,05).
Наконец, чтобы подтвердить активацию супероксиддисмутазы, которая противостоит окислительному стрессу, ученые проверили степень расширения сонной артерии при повышающихся дозах ацетилхолина после введения миметика супероксиддисмутазы 4-гидрокси-2,2,6,6-тетраметилпиперидин-1-оксид (ТЕМПОЛ). ТЕМПОЛ восстанавливал эндотелиально зависимое расширение сонных артериях у мышей, которых кормили пищей с добавлением ТМАО, до уровня, наблюдаемого в контрольной группе (р < 0,05), но он не оказывал влияния на расширение артерий у мышей из контрольной группы. Таким образом, ученые показали, что ТМАО ухудшает биодоступность оксида азота за счет его разрушения в реакциях окислительного стресса, а также, возможно, снижения работы eNOS. ТМАО ухудшал функцию эндотелия сосудов, способствуя развитию супероксидного окислительного стресса, в отсутствие явного повышения провоспалительной сигнализации и экспрессии цитокинов.
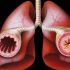
Количество белка P-eNOS (фосфорилированная эндотелиальная синтаза оксида азота), оцениваемое по иммунофлюоресценции в стенках аорты.
Brunt et al. / Hypertension, 2020
Поделиться
Плазменные концентрации ТМАО были выше у людей среднего и старшего возраста (50-79 лет) по сравнению с молодыми (18-27 лет) взрослыми (р < 0,001). Концентрация холина — предшественника ТМАО — в плазме крови также была выше у людей старшего возраста (р < 0,001), а концентрации L-карнитина и бетаина были примерно равны. Следует отметить, что в диете молодых и пожилых людей не было значимых различий.
Степень расширения артерии под действием потока крови напрямую зависит от сохранности функции эндотелия сосудов. Он реагирует на увеличившееся давление крови и выделяет оксид азота, который увеличивает просвет сосуда, снижая давление крови. По степени расширения плечевой артерии под действием потока крови ученые оценивали сохранность функции эндотелия у людей. Выяснилось, что эндотелиальная функция была достоверно ниже у людей старшего возраста (р < 0,0001) при одинаковых исходных диаметрах плечевой артерии (р = 0,70).
Концентрация TMAO в плазме крови обратно пропорциональна эндотелиальной функции у здоровых взрослых людей в разном возрасте. ТМАО плазмы (А) и эндотелиальная функция (В) у молодых (N = 19) и пожилых (MA/O; N = 98) взрослых
Ученые обнаружили, что степень расширения плечевой артерии под действием потока крови обратно связана с концентрацией ТМАО в плазме крови (р < 0,00001). При корректировке модели с учетом возраста и пола эта связь оставалась значимой (р < 0,0001), а также когда модель корректировалась с учетом возраста, пола, индекса массы тела, систолического артериального давления, общего холестерина сыворотки крови, липопротеидов низкой плотности и глюкозы крови натощак (р < 0,0001). Это указывает на то, что повышенные концентрации TMAO ведут к эндотелиальной дисфункции независимо от традиционных факторов риска сердечно-сосудистых заболеваний. Половых различий в соотношении между ТМАО и степенью расширения плечевой артерии не наблюдалось (р = 0,42). При этом взаимосвязи между возрастными изменениями концентрации ТМАО в плазме и функцией эндотелия с приемом антигипертензивных препаратов обнаружено не было.
Также ученые обнаружили агент, снижающий концентрацию ТМАО плазме крови мышей. Им оказался 3,3-диметил-1-бутанол — структурный аналог холина. Он ингибирует микробную ТМА-лиазу и препятствует превращению холина и других предшественников в ТМА кишечной микробиотой. 3,3-диметил-1-бутанол снижал уровень ТМАО в плазме крови старых мышей до уровня, наблюдаемого у молодых мышей (р = 0,99), но не оказывал влияния на уровень ТМАО в плазме крови молодых мышей (р = 0,99).
Таким образом, ученые продемонстрировали прямую связь возрастной эндотелиальной дисфункции как у мышей, так и у здоровых людей, с высокой концентрацией метаболита кишечного микробиома триметиламиноксида в плазме крови. Пагубное влияние этого вещества заключается в активации окислительного стресса, который снижает биодоступность естественного «расширителя» сосудов — оксида азота. Это создает предпосылки к развитию атеросклероза и артериальной гипертензии, которые ведут к различным заболеваниям сердечно-сосудистой системы.
Недавно мы рассказывали про развитие одного из факторов риска сердечно-сосудистых заболеваний, к которому ведет эндотелиальная дисфункция — атеросклероз. Оказалось, что атеросклеротические бляшки могут появляться при частых ночных пробуждениях.
Вячеслав Гоменюк
https://nplus1.ru/




Нет комментариев
Оставте комментарий